اوره، در متابولیسم ترکیبات حاوی نیتروژن در بدن حیوانات نقش مهمی ایفا میکند و در عین حال، ماده اصلی حاوی نیتروژن، در ادرار پستانداران به شمار میآید. این ترکیب: سخت، بیرنگ، بیبو است (گر چه آمونیاکی که در حضور آب از آن حاصل میشود و شامل بخار آب موجود در هوا نیز میباشد، بوی تندی دارد)، نه اسیدی است و نه قلیایی، بسیار محلول در آب و نسبتاً غیر سمی میباشد، از اوره به صورت گستردهای در کودهای شیمیایی به عنوان یک منبع غنی و مناسب نیتروژن استفاده میشود. اوره همچنین یکی از مواد اولیه مهم در صنایع شیمیایی است. سنتز و به وجود آوردن این ترکیب آلی از یک پیش ساز غیرآلی یا معدنی، توسط فریدریش وهلر Friedrich Wöhler در سال ۱۸۲۸، نقطه عطف بسیار مهمی در توسعه و پیشرفت دانش شیمی محسوب میشود.
اوره برای نخستین بار، به سال ۱۷۷۳ میلادی توسط شیمیدان فرانسوی به نام هیلاری رول Hilaire Rouelle درون ادرار کشف گردید. در سال ۱۸۲۸ میلادی، شیمیدان آلمانی فریدریش وهلر، طی تلاشی ناموفق برای تهیه کردن سیانات آمونیم، و هنگامیکه به ایزوسیانات نقره، کلرید آمونیوم اضافه کرد، اوره بدست آورد: این اولین باری بود که یک ترکیب آلی به صورت مصنوعی از مواد پیش ساز غیرآلی (معدنی) سنتز میگردید، بدون این که ارگانیسمها یا موجودات زنده، هیچگونه دخالتی در این روند داشته باشند. درک همین موضوع، نقش بسیار مهمی در توسعه شیمی آلی ایفا نمود. بسیاری معتقدند که وهلر را باید به خاطر همین اکتشاف، پدر شیمی آلی در نظر گرفت.
بیشتر از ۹۰ ٪ از تولید اوره در دنیا، به منظور استفاده به عنوان کودهای شیمیایی حاوی نیتروژن است. در کاربردهای عمومی، اوره دارای بالاترین مقدار ازت در میان تمامی کودهای جامد نیتروژنی میباشد (۴۶٫۷ ٪). بر این اساس، اوره پایینترین هزینههای حمل و نقل را به ازای هر واحد از تغذیه نیتروژنی به بار میآورد. اوره در خاک، هیدرولیز شده و به آمونیاک و دی اکسید کربن مبدل میگردد. آمونیاک حاصل از این فرایند، توسط باکتریهای موجود در خاک به نیترات اکسیده میشود، و در نتیجه میتواند توسط گیاه جذب گردد. اوره همچنین در بسیاری از موارد، در فرمولاسیون چند جزئی کودهای جامد نیز، مورد استفاده واقع میشود. اوره به طور معمول، به میزان بین ۴۰ تا ۳۰۰ کیلوگرم به ازای هر هکتار در اراضی کشاورزی پخش میگردد، اوره را میتوان به صورت خشک به خاک افزود، و یا آن را به صورت محلول و از طریق آب آبیاری به کار برد. فرایند انحلال اوره در آب یک فرایند اندومتریک است که باعث افت دمای محلول در هنگام حل شدن اوره میشود.
اوره در واکنشهای SNCR و SCR به منظور کاهش آلایندههای No دار، که در گازهای حاصل از احتراق موجود هستند، کاربرد دارد. به عنوان مثال، گازهایی که از نیروگاهها و یا از موتورهای دیزلی خارج میشوند. در مورد موتورهای دیزلی، این فرایند به نام فیلتر بازسازی ذرات دیزلی خوانده میشود. در مورد سیستم های بلوتک BlueTec، به عنوان مثال، از تزریق اوره محلول در آب به سیستم اگزوز خودرو استفاده میشود. آمونیاک حاصل شده از فرایند تجزیه اوره، با اکسید نیتروژن خروجی واکنش داده و توسط یک مبدل کاتالیزوری، به نیتروژن و آب تبدیل میشود.
آمونیاک
آمونیاک ( Ammonia ) با فرمول شيميايي NH3،مهمترین ترکیب هیدروژنه ازت (نیتروژن) است که در طبیعت از تجزیه مواد آلی ازت دار همچون اوره ادرار به دست میآید. آمونیاک گازی است بی رنگ، با مزه فوق العاده تند و طعم حاد و زننده که اشکآور و خفه کننده است. گاز آمونیاک از هوا سبک تر بوده و به سهولت به مایع تبدیل میشود. آمونیاک در آب بسیار محلول بوده و در منفی 77.7 درجه سانتیگراد منجمد و در منفی 33.34 درجه سانتیگراد به جوش میآید. وزن مخصوص محلول اشباع آمونیاک 0.88 گرم بر سانتیمتر مکعب است.
گاز آمونیاک قابل افروزش بوده و حدود اشتعالش ۱۶-۲۵ درصد حجمی گاز آمونیاک در هوا است. حضور مواد نفتی و دیگر مواد افروختنی خطر آتشگیری را افزایش میدهد. گاز آمونیاک در گرمای ۴۰۰ درجه به بالا تجزیه شده و تولید هیدروژن و نیتروژن میکند. از موارد استفاده آمونياك مى توان به استفاده در تهيه ى كود هاى شيميايى ( کودهای نیتراته و فسفاته ) تهیه اسید نیتریک، گاز مبرد در دستگاه های خنک کننده و تولید مواد منفجره اشاره كرد .
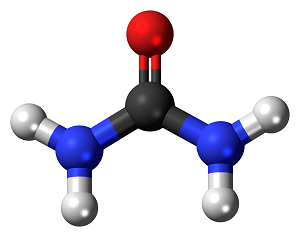 اوره
اوره 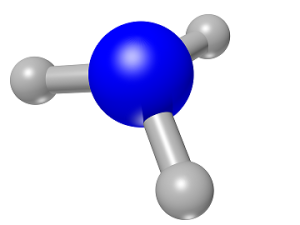 آمونیاک
آمونیاک